Тартар қышқылы
Бұл мақала әлі тексерістен өтпеді. Тексерілмеген мақалалардағы мәліметтер сенімсіз болуы мүмкін.
|
Тартар қышқылы - табиғи түрде көптеген жемістерде, әсіресе жүзімде, сонымен қатар банандарда, тамариндерде және цитруста кездесетін ақ, кристалды органикалық қышқыл . [1] Оның тұзы, калий битартраты, әдетте татар кремі ретінде белгілі, ашыту процесінде табиғи түрде дамиды. Ол әдетте натрий бикарбонатымен араласады және тағам дайындауда қопсытқыш ретінде пайдаланылатын пісіру ұнтағы ретінде сатылады. Қышқылдың өзі тағамға E334 антиоксиданты ретінде және оның ерекше қышқыл дәмін беру үшін қосылады. Табиғи жағдайда кездесетін шарап қышқылы органикалық химиялық синтезде пайдалы шикізат болып табылады. Тартар қышқылы - альфа-гидрокси-карбон қышқылы, қышқылдық сипаттамалары бойынша дипротикалық және альдарлық және янтарь қышқылының дигидроксил туындысы.
Тарих[өңдеу | қайнарын өңдеу]
Тартар қышқылы ғасырлар бойы шарапшыларға белгілі болды. Алайда экстракцияға арналған химиялық процесті 1769 жылы швед химигі Карл Вильгельм Шееле әзірледі.[2]
Химиялық хирализмді ашуда шарап қышқылы маңызды рөл атқарды. Бұл қасиетін шарап қышқылы алғаш рет 1832 жылы Жан Батист Био байқаған, ол оның поляризацияланған жарықты айналдыру қабілетін байқаған.[3] [4] Луи Пастер бұл зерттеуді 1847 жылы хиральды деп тапқан натрий аммоний тартратының кристалдарының пішіндерін зерттеу арқылы жалғастырды. Әртүрлі пішіндегі кристалдарды қолмен сұрыптау арқылы Пастер бірінші болып левотартар қышқылының таза үлгісін шығарды.[5] [6] [7] [8] [9]
Стереохимия[өңдеу | қайнарын өңдеу]
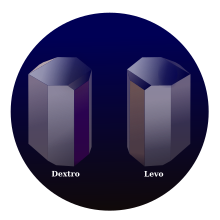
Қышқылдың табиғи түрі - декстро-тартарикалық қышқыл немесе L-(+)-тартарикалық қышқыл (ескірген атауы "mwTAd-тартар қышқылы). Табиғи түрде қол жетімді болғандықтан, ол өзінің энантиомеріне және мезоизомеріне қарағанда арзанырақ. Декстро және лево префикстері архаикалық терминдер.[10] Қазіргі оқулықтарда табиғи түрге (2R, 3R)-шалба қышқылы (L-(+)-тартар қышқылы), ал оның энантиомеріне (2S,3S)-тартар қышқылы (D -(-)- деп жатады. шарап қышқылы). Мезодиастереомер (2R, 3S ) - шарап қышқылы немесе (2S,3R) - шарап қышқылы деп аталады.
- Декстро және лево моноклинді сфеноидты кристалдар[11] және орторомбты кристалдар түзеді.
- Расемикалық шарап қышқылы моноклиникалық[12] және триклиникалық кристалдар түзеді (кеңістік тобы P1).[13] [14]
- Сусыз мезотартар қышқылы екі сусыз полиморфты құрайды: триклиндік және орторомбты.
- Моногидратталған мезотартар қышқылы сулы ерітіндіден кристалдану орын алатын температураға байланысты моноклиникалық және триклиндік полиморфиз ретінде кристалданады.[15]
Фелинг ерітіндісіндегі шарап қышқылы мыс(II) иондарымен байланысып, ерімейтін гидроксид тұздарының түзілуіне жол бермейді.
| DL -тартар қышқылы (расем қышқылы ) (1:1 қатынасында болғанда) | мезотартар қышқылы | |
|---|---|---|
| декстротартар қышқылы (L-(+)-тартар қышқылы) |
левотартар қышқылы (D-(−)-тартар қышқылы) | |

|

|

|
| Жалпы есім | Тартар қышқылы | Левотартар қышқылы | Декстротартар қышқылы | Мезотартар қышқылы | Рацем қышқылы |
|---|---|---|---|---|---|
| Синонимдер | (2S, 3S)-тартар қышқылы (S, S)-тартар қышқылы (−)-тартар қышқылы l -тартар қышқылы (ескірген) левотартар қышқылы D - шарап қышқылыD - триар қышқылы («табиғи емес изомер»)[16] |
(2R, 3R)-тартар қышқылы (R, R)-тартар қышқылы (+)-тартар қышқылы d -тартар қышқылы (ескірген) L - шарап қышқылы L - триар қышқылы («табиғи изомер») [17] |
(2R, 3S)-тартар қышқылы мезо -тартар қышқылы эритра қышқылы |
rac-(2R, 3S)-тартар қышқылы (2RS, 3SR)-тартар қышқылы (±)-тартар қышқылы DL - шарап қышқылы dl -тартар қышқылы (ескірген) паратартар қышқылы увин қышқылы | |
| PubChem | CID 875 | PubChem CID 439655 | PubChem CID 444305 | PubChem CID 78956 | CID 5851 |
| EINECS нөмірі | 205-695-6 | 201-766-0 | 205-696-1 | 205-105-7 | |
| CAS нөмірі | 526-83-0 | 147-71-7 | 87-69-4 | 147-73-9 | 133-37-9 |
Өндіріс[өңдеу | қайнарын өңдеу]
L-(+)-Татар қышқылы[өңдеу | қайнарын өңдеу]
Татар қышқылының L-(+)-шайыр қышқылы изомері өнеркәсіпте ең көп мөлшерде өндіріледі. Ол ашытудың қатты жанама өнімі болып табылатын лизден алынады. Бұрынғы жанама өнімдер негізінен калий битарратынан (KHC4H4O6) тұрады. Бұл калий тұзы кальций гидроксиді «әк сүтімен» (Ca(OH)2) өңдеу кезінде кальций тартратына (CaC4H4O6) айналады:
Іс жүзінде кальций хлоридін қосқанда кальций тартратының жоғары шығымдылығы алынады. Содан кейін кальций тартраты тұзды сулы күкірт қышқылымен өңдеу арқылы шарап қышқылына айналады:
Расемикалық шарап қышқылы[өңдеу | қайнарын өңдеу]
Рацемикалық шарап қышқылын малеин қышқылынан көп сатылы реакцияда дайындауға болады. Бірінші қадамда малеин қышқылы катализатор ретінде калий вольфратын пайдаланып сутегі асқын тотығымен эпоксидантылады.
- HO2CC2H2CO2H + H2O2 → OC2H2(CO2H)2
Келесі қадамда эпоксид гидролизденеді.
- OC2H2(CO2H)2 + H2O → (HOCH)2(CO2H)2
мезо-тартар қышқылы[өңдеу | қайнарын өңдеу]
Рацемиялық қышқыл мен мезотартар қышқылының қоспасы декстротартар қышқылы суда шамамен 2 күн бойы 165 °C температурада қызған кезде пайда болады.[18]
- HO2CCHBrCHBrCO2H + 2AgOH → HO2CCH(OH)CH(OH)CO2H + 2AgBr
мезо-тартар қышқылын қалдық рацем қышқылынан кристалдану арқылы бөлуге болады, рацемат аз ериді.
Реактивтілік[өңдеу | қайнарын өңдеу]
L-(+)-тартар қышқылы, бірнеше реакцияларға қатыса алады. Төмендегі реакция схемасында көрсетілгендей, дигидроксималеин қышқылы L-(+)-тартар қышқылын темір тұзының қатысуымен сутегі асқын тотығымен өңдеген кезде түзіледі.
- HO2CCH(OH)CH(OH)CO2H + H2O2 → HO2CC(OH)C(OH)CO2H + 2H2O
Содан кейін дигидроксималеин қышқылын азот қышқылымен тартрон қышқылына дейін тотықтыруға болады.[19]
Туындылар[өңдеу | қайнарын өңдеу]


Татар қышқылының маңызды туындыларына оның тұздары, татар кілегейі (калий битарраты), Рошель тұзы (калий натрий тартраты, жұмсақ іш жүргізгіш) және татар эметикасы (калийдің сурьмасы) жатады.[20] [21] [22] Диизопропил тартрат асимметриялық синтезде кокатализатор ретінде қолданылады.
Татар қышқылы - алма қышқылының өндірісін тежеу арқылы жұмыс істейтін бұлшықет токсині және жоғары дозада паралич пен өлімге әкеледі. Орташа өлім дозасы (LD50) адам үшін шамамен 7,5 грамм/кг құрайды, 5,3 қояндар үшін грамм/кг, ал 4,4 тышқандар үшін грамм/кг. Бұл көрсеткішті ескерсек, ол 500 граммден асады салмағы 70 килограмм адамды өлтіру, сондықтан оны көптеген тағамдарға, әсіресе қышқыл дәмі бар тәттілерге қауіпсіз түрде қосуға болады. Азық-түлік қоспасы ретінде шарап қышқылы антиоксидант ретінде пайдаланылады E саны E334; Тартраттарантиоксиданттар немесе эмульгаторлар ретінде қызмет ететін басқа қоспалар.
Суға татар кремін қосқанда, суспензия пайда болады, ол мыс монеталарын өте жақсы тазартуға қызмет етеді, өйткені тартрат ерітіндісі монета бетіндегі мыс(II) оксидінің қабатын еріте алады. Алынған мыс(II)-тартрат кешені суда оңай ериді.
Шараптағы шарап қышқылы[өңдеу | қайнарын өңдеу]

Тартар қышқылы шарап ішетіндерге «шарап алмаздарының», кейде бөтелкенің тығынында немесе түбінде өздігінен пайда болатын шағын калий битартраты кристалдарының көзі ретінде бірден танылуы мүмкін. Бұл «тартраттар» кейде шыны сынған деп қателескеніне қарамастан зиянсыз және көптеген шараптарда салқын тұрақтандыру арқылы алдын алады (бұл шараптың профилін өзгерте алатындықтан әрқашан артықшылық бермейді). Қартаю бөшкелерінің ішкі жағында қалған тартраттар бір уақытта калий битарратының негізгі өнеркәсіптік көзі болды.
Тартар қышқылы химиялық маңызды рөл атқарады, ашытудың рН деңгейін көптеген жағымсыз бұзылатын бактериялар өмір сүре алмайтын деңгейге дейін төмендетеді және ашытудан кейін консервант ретінде әрекет етеді. Ауыз қуысында шараптың ащылығын қамтамасыз етеді, бірақ лимон және алма қышқылдары да рөл атқарады.
Цитрустағы шарап қышқылы[өңдеу | қайнарын өңдеу]
Зерттеу нәтижелері цитрус жемістерінде органикалық егіншілікте өндірілген жемістерде кәдімгі ауыл шаруашылығында өндірілген жемістерге қарағанда шарап қышқылының жоғарырақ болатынын көрсетті.[23]
Қолданбалар[өңдеу | қайнарын өңдеу]
Тартар қышқылы және оның туындылары фармацевтика саласында кең көлемде қолданылады. Мысалы, лимон қышқылымен бірге көпіршікті тұздар өндірісінде ауызша дәрілердің дәмін жақсарту үшін қолданылған. Татар эметикасы деп аталатын қышқылдың калий антимонил туындысы аз мөлшерде жөтел сиропына қақырық түсіретін дәрі ретінде қосылады.
Тартар қышқылының өнеркәсіптік қолдану үшін бірнеше қосымшалары бар. Қышқылдың кальций және магний сияқты металл иондарын хелатизациялауы байқалды. Сондықтан қышқыл ауылшаруашылық және металл өнеркәсібінде топырақ тыңайтқышындағы микроэлементтерді комплексті ету және сәйкесінше алюминий, мыс, темір және осы металдардың қорытпаларынан тұратын металл беттерін тазалау үшін хелаттандырушы агент ретінде қызмет етті.
Иттердегі уыттылық[өңдеу | қайнарын өңдеу]
Татар қышқылы адамдар мен зертханалық жануарларға жақсы төзімді болғанымен, 2021 жылдың сәуір айында JAVMA редакторына жіберілген хатта жүзімдегі шарап қышқылы иттердегі жүзім мен мейіздің уыттылығының себебі болуы мүмкін деген болжам жасалды.[24]
Дереккөздер[өңдеу | қайнарын өңдеу]
- ↑ Duarte, A.M.; Caixeirinho, D.; Miguel, M.G.; Sustelo, V.; Nunes, C.; Fernandes, M.M.; Marreiros, A. (2012). "Organic acids concentration in citrus juice from conventional versus organic farming". Acta Horticulturae (933): 601–606. https://www.actahort.org/books/933/933_78.htm.
- ↑ Retzius, Anders Jahan (1770) "Försök med vinsten och dess syra" (Experiments with cream of tartar and its acid), Kungliga Vetenskapsakademiens Handlingar (Proceedings of the Royal Academy of Sciences), 31 : 207–213. From p. 209: "§. 6. Dessa försök omtalte jag för Hr. Carl Wilhelm Scheele (en snabb och lårgirug Pharmaciæ Studiosus) … " (§. 6. I mention these experiments on behalf of Mr. Carl Wilhelm Scheele (a quick and studious student of pharmacology) … )
- ↑ Biot (1835) "Mémoire sur la polarization circulaire et sur ses applications à la chimie organique" (Memoir on circular polarization and on its applications to organic chemistry), Mémoires de l'Académie des sciences de l'Institut, 2nd series, 13 : 39–175. That tartaric acid (acide tartarique cristallisé) rotates plane-polarized light is shown in Table G following p. 168. (Note: This article was read to the French Royal Academy of Sciences on 1832 November 5.)
- ↑ Biot (1838) "Pour discerner les mélanges et les combinaisons chimiques définies ou non définies, qui agissent sur la lumière polarisée; suivies d'applications aux combinaisons de l'acide tartarique avec l'eau, l'alcool et l'esprit de bois" (In order to discern mixtures and chemical combinations, defined or undefined, which act on polarized light; followed by applications to combinations of tartaric acid with water, alcohol [i.e., ethanol], and spirit of wood [i.e., methanol]), Mémoires de l'Académie des sciences de l'Institut, 2nd series, 15 : 93–279.
- ↑ L. Pasteur (1848) "Mémoire sur la relation qui peut exister entre la forme cristalline et la composition chimique, et sur la cause de la polarisation rotatoire" (Memoir on the relationship which can exist between crystalline form and chemical composition, and on the cause of rotary polarization)," Comptes rendus de l'Académie des sciences (Paris), 26 : 535–538.
- ↑ L. Pasteur (1848) "Sur les relations qui peuvent exister entre la forme cristalline, la composition chimique et le sens de la polarisation rotatoire" (On the relations that can exist between crystalline form, and chemical composition, and the sense of rotary polarization), Annales de Chimie et de Physique, 3rd series, 24 : 442–459.
- ↑ Pasteur, Louis (1850) "Recherches sur les propriétés spécifiques des deux acides qui composent l'acide racémique" [Investigations into the specific properties of the two acids that compose racemic acid], Annales de Chimie et de Physique, 3rd series, 28 (3) : 56–99. See also Plate II. (See also the report of the commission that was appointed to verify Pasteur's findings, pp. 99–117.) [in French]
- ↑ George B. Kauffman and Robin D. Myers (1998). "Pasteur's resolution of racemic acid: A sesquicentennial retrospect and a new translation". The Chemical Educator 3 (6): 1–4. http://192.129.24.144/licensed_materials/00897/papers/0003006/36kau897.pdf.
- ↑ Flack, H.D. (2009). "Louis Pasteur's discovery of molecular chirality and spontaneous resolution in 1848, together with a complete review of his crystallographic and chemical work". Acta Crystallographica A 65 (5): 371–389. doi:10.1107/S0108767309024088. http://crystal.flack.ch/sh5092.pdf.
- ↑ Lecture 28: Stereochemical Nomenclature; Racemization and Resolution | CosmoLearning Chemistry. CosmoLearning.
- ↑ W, T, Astbury (Feb 1923). "The Crystalline Structure and Properties of Tartaric Acid". Proc. Royal Soc. A 102 (718): 506–528. Bibcode 1923RSPSA.102..506A. https://royalsocietypublishing.org/doi/pdf/10.1098/rspa.1923.0010., based on P. Groth’s “Chemische Krystallographie".
- ↑ CRC Handbook of Chemistry and Physics, 49th edition.
- ↑ Samantha Callear and Michael Hursthouse D-Tartaric acid. Crystallography Open Database (2008).
- ↑ Paul Luner (Jul 2002). "(+-)-Tartaric acid". Acta Crystallographica Section C 58 (6): o333–o335. https://www.researchgate.net/publication/11324000., (±)-Tartaric acid. Crystallography Open Database (2002).
- ↑ G. A. Bootsma and J. C. Schoone (1967). "Crystal Structures of Meso Tartaric Acid". Acta Crystallogr. 22 (4): 522–532. https://scripts.iucr.org/cgi-bin/paper?a05502.
- ↑ d-Tartaric acid. PubChem.
- ↑ L-(+)-Tartaric acid. PubChem. Басты дереккөзінен мұрағатталған 16 мамыр 2015.
- ↑ Augustus Price West. Experimental Organic Chemistry. World Book Company: New York, 1920, 232-237.
- ↑ Blair, G. T.; DeFraties, J. J. (2000). "Hydroxy Dicarboxylic Acids". Kirk Othmer Encyclopedia of Chemical Technology. pp. 1–19.
- ↑ Zalkin, Allan; Templeton, David H.; Ueki, Tatzuo (1973). "Crystal structure of l-tris(1,10-phenathroline)iron(II) bis(antimony(III) d-tartrate) octahydrate". Inorganic Chemistry 12 (7): 1641–1646. doi:10.1021/ic50125a033.
- ↑ Haq, I; Khan, C (1982). "Hazards of a traditional eye-cosmetic--SURMA". The Journal of the Pakistan Medical Association 32 (1): 7–8.
- ↑ McCallum, RI (1977). "President's address. Observations upon antimony". Proceedings of the Royal Society of Medicine 70 (11): 756–63. doi:10.1177/003591577707001103.
- ↑ Duarte, A.M.; Caixeirinho, D.; Miguel, M.G.. "Organic Acids Concentration in Citrus Juice from Conventional Versus Organic Farming". Acta Horticulturae (933): 601–606. doi:10.17660/actahortic.2012.933.78.
- ↑ McReynolds What causes grape toxicity in dogs? Playdough might have led to a breakthrough (April 1, 2021).

