Аминдер
| Бірінші амин | Екінші амин | Үшінші амин |
|---|---|---|
 |
 |
 |
Аминдер — молекуласындағы бір немесе бірнеше сутек атомы амин тобына (-NH2) алмасқан көмірсутектердің туындылары. Амин тобымен байланысқан радикалдың табиғатына байланысты аминдер алифатты және ароматты болып бөлінеді.Аминдерді аммиактағы сутек атомдарының орнын радикал басқан аммиактың туындылары деп те қарастыруға болады.
Молекуласындағы амин тобының санына байланысты аминдер: моноаминдер, диаминдер және полиаминдер болып бөлінеді.[1]
Толығырақ
[өңдеу | қайнарын өңдеу]Аминдер радикалдық санына байланысты бірінші, екінші және үшінші Аминдер деп бөлінеді. Аминдердің алкиламиндер және ароматтық Аминдер (ариламиндер) деген түрлері бар. Алкиламиндер – күшті, ариламиндер – әлсіз негіздер. Алкиламиндер минералды қышқылдармен әрекеттескенде көп жағдайда суда жақсы еритін тұздар түзеді. Тас көмір қышқылдарымен, олардың ангидридтерімен, күрделі эфирлермен қыздырғанда бірінші және екінші Аминдердегі сутек атомы алмасқан амидтер түзіп ацилденеді. Аминдерді анықтау үшін олардың амидтерге ацилдену реакциясын пайдаланады. Аминдердің көпшілігі табиғатта кездеседі. Физиол. белсенділігі олардың сутекті, ковалентті, иондық байланыстар түзуіне негізделген. Аминдер өсімдіктер дүниесінде әр түрлі процестерде (метаболизм, т.б.) маңызды рөл атқарады. Сондай-ақ синтетик. жолмен алынған Аминдердің емдік қасиеттері бар. Осыған байланысты Аминдер бактериялық құрт ауруларын емдеуде кеңінен қолданылады.Аминдер радикалдық санына байланысты біріншілік RNH2, екіншілік R2NH және үшіншілік R3N болып бөлінеді.[2]
Атаулары мен изомерлері
[өңдеу | қайнарын өңдеу]Халықаралық (ИЮПАК) атау жүйесі бойынша көмірсутектерді нөмірлеп, көмірсутектердің атына амин, диамин немесе триамин деген сөз қосып атайды. Аминдерге көміртек қаңқасының және функционалдық топтың орнына байланысты изомерлену тән.[1]
Алу жолдары
[өңдеу | қайнарын өңдеу]1. Аминдерді нитроқосылыстарды катализатор (Pt, Pd, Ni) қатысында тотықсыздандырып алады:
- R – NO2 + 3H2 → R – NH2 + 2H2O
Өндірісте анилинді алу нитробензолды катализатор (Pd, Pt, Ni) қатысында тотықсыздандыруға негізделген:
C6H5NO2 + 3H2 → C6H5NH2 + 2Н2O
Н.Н. Зинин (1842 жылы) нитробензолды күкіртсутекпен тотықсыздандырып, анилин алған:
Нитробензолды шойын жоңқасы мен тұз қышқылы қатысында тотықсыздандырып та алады. Атом күйінде сутек бөлініп, ол нитробензолды тотықсыздандырады:[1]
- Fе + 2HCl → FеСl2 + 2Н
- C6H5 - NO2+ 6Н → C6H5 - NH2 + 2Н2O
Физикалық қасиеттері және құрылысы
[өңдеу | қайнарын өңдеу]Қарапайым алифатты аминдер (метиламин, этиламин, диметиламин) газ тәрізді заттар, суда жақсы ериді. Иістері аммиактың иісіне ұқсас. Ортаңғы аминдер сұйық заттар, иістері балықтың иісін еске түсіреді. Құрамында көміртек атомы көп аминдер — иіссіз, қатты заттар. Көміртек тізбегіндегі көміртектің саны өскен сайын суда ерігіштігі төмендейді. Аминдер органикалық, еріткіштерде (бензол, т.б.) жақсы ериді. Анилин түссіз май тәрізді, улы зат. Суда нашар ериді, ал органикалық еріткіштерде жақсы ериді. Ауада тотығып, қоңыраяды.
Аминдер қасиеттерінің аммиакқа үқсас болуы, олардың электрондық құрылысымен түсіндіріледі.
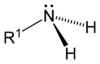
Аммиак молекуласында азот атомының үш электроны ковалентті байланыс түзуге жұмсалады да, жұп электроны бос болады. Аминдер молекуласының құрылысы да аммиакқа ұқсас, азоттың үш электроны коваленттік байланыста болады, ал бір электрон жұбы бос болады:[1]

Аминдердің химиялық қасиеттері
[өңдеу | қайнарын өңдеу]Аминдер аммиакқа ұқсас негіздік қасиет көрсетеді. Аминдердің негіздік қасиеті — аммиактан жоғары. Себебі аммиакта үш сутек атомының электрон бұлттары азотқа қарай ығысады, ал алкиламиндерде, мысалы, метиламинде екі сутек атомы тікелей жоне үш сутек көміртектің атомы арқылы барлығы бес сутектің электрондары азотқа қарай ығысады. Осының әсерінен метиламинде азот атомындағы теріс зарядтың мөлшері аммиактағы азот атомына қарағанда жоғары болады:

Теріс заряды көп болғандықтан, амин молекуласындағы азот атомы протон қосып алуға бейім болады да, негіздік қасиет көрсетеді.[1]
Аминдердің протон қосып алуы
[өңдеу | қайнарын өңдеу]Аминдер сулы ерітінділерінде аммиак сияқты оң зарядталған сутек ионын (протонды) қосып алып, аммонийлі қосылысқа айналады. Ерітіндіде гидроксил иондары босап, сілтілік орта береді, лакмусты көк түске, фенолфталеинді таңқурай түске бояйды.[1]
Анилин (фениламин)
[өңдеу | қайнарын өңдеу]Анилиннің формуласын әр түрлі жазуға болады:
Анилин қаныққан көмірсутектердің аминдері сияқты қышқылдармен әрекеттесіп тұз түзгенімен, сулы ерітіндісінде лакмустың түсін өзгертпейді. Яғни, қаныққан көмірсутектердің аминдерінен анилиннің негіздік қасиеті әлсіз болғаны.
Бұл құбылысты анилин молекуласындағы атом топтарының өзара әсері арқылы түсіндіруге болады. Фенол молекуласындағы сияқты бензол сақинасы аминтобындағы азоттың бос электрон жұбын өзіне тартады. Азот атомының электрон тығыздығы азайғандықтан, оның протонды өзіне тартуы кеміп, негіздік қасиеті төмендейді. Анилин химиялық реакцияларға амин тобы жәнө бензол ядросы бойынша түседі.[1]
Аминдердің жеке өкілдері және олардың қолданылуы
[өңдеу | қайнарын өңдеу]Метиламин CH3NH2— өткір иісті, түссіз газ. Иісі аммиактың иісіне ұқсас. Суда жақсы ериді, қанық ерітіндіде 35—40% метиламин болады.
Өндірісте метиламинді көгерткіш қышқылды катализатор қатысында тотықсыздандырып алады:
- Н-C≡N + 2Н2 → CH3-NH2
Органикалық синтезде метиламинді дәрі-дәрмектер алу үшін қолданады. Сонымен қатар метиламиннен бояғыш заттар және беттік белсенді қосылыстар алынады.
Гексаметилендиамин Н2N(CH2)6NH2 — түссіз кристалды зат, суда ериді.
Гексаметилендиамин полиамидтер және синтездік талшық — нейлон алу үшін қолданылады.
Анилин C6H5NH2— өзіне тән иісі бар, түссіз майлы сұйықтық. Суда нашар ериді, спирт, эфир, бензол сиякты органикалық еріткіштерде жақсы ериді. Анилинге тотықтырғыштармен әсер еткенде, түстері әр түрлі аралық бірнеше өнім (мысалы, қара анилин) түзіледі. Анилин дәрі-дәрмектер (мысалы, сульфаниламидті препараттар), қопарылғыш заттар, анилинді бояулар, антитотықтырғыштар алуда алғашқы өнім болып табылады.
Аминдерді аммиак молекуласындағы бір немесе бірнеше сутек атомдарының орнын радикал басқан аммиактың туындылары деп қарастыруға болады. Аминдер негіздік қасиет көрсетеді. Радикалдың құрылысына байланысты алифатты және ароматты болып бөлінеді. Негіздік қасиеттері осы радикалдың құрылысына байланысты болады.[1]
Дереккөздер
[өңдеу | қайнарын өңдеу]- ↑ a b c d e f g h Химия: Жалпы білім беретін мектептің жаратылыстану-математика бағытындағы 11-сыныбына арналған оқулық / Ә. Темірболатова, Н. Нұрахметов, Р. Жұмаділова, С. Әлімжанова. – Алматы: «Мектеп» баспасы, 2007. – 352 бет. ISBN 9965-36-092-8
- ↑ О.Д.Дайырбеков, Б.Е.Алтынбеков, Б.К.Торғауытов, У.И.Кенесариев, Т.С.Хайдарова Аурудың алдын алу және сақтандыру бойынша орысша-қазақша терминологиялық сөздік. Шымкент. “Ғасыр-Ш”, 2005 жыл. ISBN 9965-752-06-0
| Бұл — мақаланың бастамасы. Бұл мақаланы толықтырып, дамыту арқылы, Уикипедияға көмектесе аласыз. Бұл ескертуді дәлдеп ауыстыру қажет. |
| Бұл мақаланы Уикипедия сапа талаптарына лайықты болуы үшін уикилендіру қажет. |


