Карбонат: Нұсқалар арасындағы айырмашылық
ш Bot: Migrating 40 interwiki links, now provided by Wikidata on d:q181699 (translate me) |
ш clean up, replaced: Пайдаланылған әдебиет → Дереккөздер, таужыныс → тау жынысы (4) using AWB |
||
| 1-жол: | 1-жол: | ||
[[Сурет:Carbonate-3D-balls.png|200px|right|thumb|Карбонат]] |
[[Сурет:Carbonate-3D-balls.png|200px|right|thumb|Карбонат]] |
||
'''Көмір қышқылы''' - Н<sub>2</sub>С0<sub>3</sub> әлсіз, екі негізді, тұрақсыз қышқыл. Ол тек ерітіндіде ғана болады. Әлсіз [[Электролиттер|электролит]], [[диссоциация |
'''Көмір қышқылы''' - Н<sub>2</sub>С0<sub>3</sub> әлсіз, екі негізді, тұрақсыз қышқыл. Ол тек ерітіндіде ғана болады. Әлсіз [[Электролиттер|электролит]], [[диссоциация]]лану дәрежесі 0,17%.<ref>Химия: Усманова М. Б., Сақариянова Қ. Н. Жалпы білім беретін мектептің 9-сыныбына арналған оқулық, 2-басылымы, өңделген, толықтырылған. - Алматы: Атамұра, 2009. - 288 бет. ISBN 9965-34-929-0</ref> |
||
==Алынуы:== |
==Алынуы:== |
||
| 15-жол: | 15-жол: | ||
==Химиялық қасиеттері:== |
==Химиялық қасиеттері:== |
||
Көмір қышқылы [[индикатор |
Көмір қышқылы [[индикатор]]лар түсін өзгертеді, қышқылдарға<ref>Кристаллография, минералогия, петрография. Бұл кітап Абай атындағы Қазақтың мемлекеттік педагогты институтының, география факультетінде оқылған лекциялардың негізінде жазылды, 1990. ISBN 2—9—3 254—69</ref> |
||
тән химиялық реакцияларға түседі, екі негізді [[Қышқылдар|қышқыл]] ретінде сілтілермен орта және қышқыл тұз түзіледі: |
тән химиялық реакцияларға түседі, екі негізді [[Қышқылдар|қышқыл]] ретінде сілтілермен орта және қышқыл тұз түзіледі: |
||
: Н<sub>2</sub>С0<sub>3</sub> + NaOH = NaHC0<sub>3</sub> + Н<sub>2</sub>0 |
: Н<sub>2</sub>С0<sub>3</sub> + NaOH = NaHC0<sub>3</sub> + Н<sub>2</sub>0 |
||
| 32-жол: | 32-жол: | ||
: NaHC0<sub>3</sub> + НОН → NaOH + Н<sub>2</sub>0 + С0<sub>2</sub>↑ |
: NaHC0<sub>3</sub> + НОН → NaOH + Н<sub>2</sub>0 + С0<sub>2</sub>↑ |
||
Бұл тұз [[гидролиз |
Бұл тұз [[гидролиз]]денгенде орта ''негіздік'' болады: С(ОН ) > C(H<sup>+</sup>). |
||
====Карбонат ионына сапалық реакция:==== |
====Карбонат ионына сапалық реакция:==== |
||
| 47-жол: | 47-жол: | ||
==Таралуы== |
==Таралуы== |
||
[[Жер қыртысы |
[[Жер қыртысы]]ның шамамен 1,7%-ын (массасы бойынша) құрайды. Ең көп таралған және жынысқұрушы [[минерал]]дар қатарына жататындар — [[кальцит]] (СаС0<sub>3</sub>) және [[доломит]] (СаС0<sub>3</sub>.МgС0<sub>3</sub>). |
||
Бұлар [[әктас |
Бұлар [[әктас]]тар және [[доломит]]тер деп аталатын шөгінді карбонатты [[Тау жыныстары|тау жынысытарды]] құрайды. Аталған тау жынысытардан гөрі сирегірек ұшырасатын карбонатты тау жынысы өкілдері: |
||
* [[анкерит]] — (Са,Ғе,Мg)СО<sub>3</sub>, |
* [[анкерит]] — (Са,Ғе,Мg)СО<sub>3</sub>, |
||
* [[сидерит]] — ҒеС0<sub>3</sub>, |
* [[сидерит]] — ҒеС0<sub>3</sub>, |
||
* [[магнезит]] — МgС0<sub>3</sub>, |
* [[магнезит]] — МgС0<sub>3</sub>, |
||
* [[родохрозит]] — МnС0<sub>3</sub>. Карбонатты |
* [[родохрозит]] — МnС0<sub>3</sub>. Карбонатты тау жынысытардың өзге түрлері мүлдем сирек ұшырасады.<ref>Қазақ тілі терминдерінің салалық ғылыми түсіндірме сөздігі: Геология— |
||
Алматы: "Мектеп" баспасы", 2003.ӀSВN 5-7667-8188-1 ӀSВN 9965-16-512-2 |
Алматы: "Мектеп" баспасы", 2003.ӀSВN 5-7667-8188-1 ӀSВN 9965-16-512-2</ref> |
||
==Дереккөздер== |
|||
==Пайдаланылған әдебиет== |
|||
<references/> |
<references/> |
||
15:59, 2014 ж. сәуірдің 23 кезіндегі соңғы нұсқа
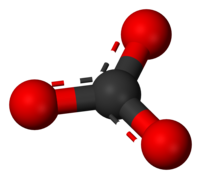
Көмір қышқылы - Н2С03 әлсіз, екі негізді, тұрақсыз қышқыл. Ол тек ерітіндіде ғана болады. Әлсіз электролит, диссоциациялану дәрежесі 0,17%.[1]
Алынуы:[өңдеу | қайнарын өңдеу]
- көмірқышқыл газын суда ерітіп
- тұзынан күшті қышқылмен әсер етіп:
Екі негізді болғандықтан сатылы диссоциацияланады:
- Н2С03↔ Н+ + НС03
- НС03- ↔ Н+ + С032-
Көмір қышқылы екі түрлі тұз түзеді, олар гидрокарбонаттар (NaHC03, Са(НС03)2) және карбонаттар деп аталады (СаС03, MgC03)
Химиялық қасиеттері:[өңдеу | қайнарын өңдеу]
Көмір қышқылы индикаторлар түсін өзгертеді, қышқылдарға[2] тән химиялық реакцияларға түседі, екі негізді қышқыл ретінде сілтілермен орта және қышқыл тұз түзіледі:
- Н2С03 + NaOH = NaHC03 + Н20
- Н2С03 + 2NaOH = Na2C03 + 2Н20
Карбонаттардың суда еритін тұздары екі сатыда гидролизденеді:[өңдеу | қайнарын өңдеу]
- : Na2C03 ↔ 2Na+ + С032-
- НОН ↔ Н+ + ОН-
- ----------------------------------
- CO32- + НОН ↔ НС03 + ОН-
- Na2C03 + НОН ↔ NaHC03 + NaOH
- NaHC03 ↔ Na+ + НС03-
- НОН ↔ Н+ + ОН-
- HC03 + НОН ↔ Н2С03+ ОН-
- ----------------------------------------
- NaHC03 + НОН → NaOH + Н20 + С02↑
Бұл тұз гидролизденгенде орта негіздік болады: С(ОН ) > C(H+).
Карбонат ионына сапалық реакция:[өңдеу | қайнарын өңдеу]
Na2C03+ Са(ОН)2 = СаС03↓ + 2NaOH Суда еритін карбонаттар әк сүтімен әрекеттесіп, ақ түсті тұнба береді.
Са2+ + С032- = СаС03↓
Қолданылуы:[өңдеу | қайнарын өңдеу]
- NaHC03 ас содасы - тамақ, шыны өндірісінде
- К2СО3 сақар - сабын алуда
- СаС03, MgC03 - құрылыс материалдары[3]
Таралуы[өңдеу | қайнарын өңдеу]
Жер қыртысының шамамен 1,7%-ын (массасы бойынша) құрайды. Ең көп таралған және жынысқұрушы минералдар қатарына жататындар — кальцит (СаС03) және доломит (СаС03.МgС03).
Бұлар әктастар және доломиттер деп аталатын шөгінді карбонатты тау жынысытарды құрайды. Аталған тау жынысытардан гөрі сирегірек ұшырасатын карбонатты тау жынысы өкілдері:
- анкерит — (Са,Ғе,Мg)СО3,
- сидерит — ҒеС03,
- магнезит — МgС03,
- родохрозит — МnС03. Карбонатты тау жынысытардың өзге түрлері мүлдем сирек ұшырасады.[4]
Дереккөздер[өңдеу | қайнарын өңдеу]
- ↑ Химия: Усманова М. Б., Сақариянова Қ. Н. Жалпы білім беретін мектептің 9-сыныбына арналған оқулық, 2-басылымы, өңделген, толықтырылған. - Алматы: Атамұра, 2009. - 288 бет. ISBN 9965-34-929-0
- ↑ Кристаллография, минералогия, петрография. Бұл кітап Абай атындағы Қазақтың мемлекеттік педагогты институтының, география факультетінде оқылған лекциялардың негізінде жазылды, 1990. ISBN 2—9—3 254—69
- ↑ “Қазақ Энциклопедиясы”
- ↑ Қазақ тілі терминдерінің салалық ғылыми түсіндірме сөздігі: Геология— Алматы: "Мектеп" баспасы", 2003.ӀSВN 5-7667-8188-1 ӀSВN 9965-16-512-2
Сыртқы сілтемелер[өңдеу | қайнарын өңдеу]
| Бұл мақаланы Уикипедия сапа талаптарына лайықты болуы үшін уикилендіру қажет. |

