Газ хроматографиясы

Газ хроматография — бұл ыдыратпай буландыруға болатын қосылыстарды бөлу үшін аналитикалық химияда қолданылатын хроматографияның кең таралған түрі. GC көбіне белгілі бір заттың тазалығын тексеру немесе қоспаның әр түрлі компоненттерін бөлу үшін қолданылады (мұндай компоненттердің салыстырмалы мөлшерін де анықтауға болады). Кейбір жағдайларда GC қосылысты анықтауға көмектеседі. Препаративті хроматографияда қоспадан таза қосылыстарды дайындау үшін GC-ді қолдануға болады.[1][2]
Газ хроматографиясында жылжымалы фаза - бұл әдетте гелий сияқты инертті немесе азот сияқты реактивті емес тасымалдаушы газ. Бөлу үшін сутек газы тиімді болғанымен, гелий құралдардың 90% қолданылатын кең таралған тасымалдаушы газ.[3] Стационарлы фаза ретінде көбіне баған деп аталатын әйнектен немесе металлдан жасалған түтіктің ішкі қабырғасынадағы инертті қатты тіректегі сұйықтықтың немесе полимердің микроскопиялық қабаты қолданылады. Газ хроматографиясын жүргізу үшін қолданылатын құрал газ хроматограф (немесе «аэрограф», «газ сепараторы») деп аталады.
Талданатын газ қосылыстар стационарлы фазамен қапталған бағанның қабырғаларымен әрекеттеседі. Қоспадағы әр қосылыс тежелу уақыты деп аталатын белгілі бір уақытта элюцияланады (шайылып шағады). Тежелу уақытын салыстыру GC-ге оның аналитикалық тиімділігін береді.
Газды хроматография принципі бойынша бағанды хроматографияға ұқсас (хроматографияның басқа түрлері сияқты, мысалы, HPLC), бірақ бірнеше маңызды айырмашылықтары бар. Біріншіден, қоспадағы қосылыстарды бөлу процесі сұйық стационарлы фаза мен жылжымалы газ фазасы арасында жүреді, ал бағанды хроматографияда стационарлы фаза қатты, ал жылжымалы фаза сұйық болып табылады. Демек, процедураның толық атауы - «Газ-сұйық хроматографиясы» - сәйкесінше мобильді және стационарлы фазаларды атайды. Екіншіден, баған газдың температурасын басқаруға болатын пеште орналасқан, ал әдеттегі бағанды хроматографияда температура бақылауы жоқ. Және үшіншіден, газ фазасындағы қосылыстың концентрациясы тек газдың бу қысымының функциясы.[1]
Газ хроматографиясы кейде бу фазалы хроматография (VPC) немесе газ-сұйықты таралу хроматографиясы (GLPC) деп те аталады. Бұл балама атаулар, сондай-ақ олардың қысқартулары ғылыми әдебиетте жиі қолданылады. Нақтырақ айтсақ, GLPC - бұл ең дұрыс термин, сондықтан көптеген авторлар осыны таңдайды.[1]
Тарихы[өңдеу | қайнарын өңдеу]
Хроматография орыс ғалымы Михаил Семенович Цветтің[4] 1903 жылғы сұйық хроматография көмегімен өсімдік пигменттерін бөлген эксперименттеріне негізделген. Неміс химигі Эрика Кремер 1947 жылы аустриялық докторант Фриц Приормен бірге GC-дің теориялық негіздерін жасап, алғашқы сұйық-газды хроматографты жасады, бірақ оның жұмысы маңызды емес болып саналды және ұзақ уақыт бойы еленбеді.[5] Арчер Жон Портер Мартин сұйық-сұйық (1941) және қағаз (1944) хроматографиясын дамыту жұмысы үшін Нобель сыйлығына ие болды, сондықтан газ хроматографиясының негізін қалады деп есептеледі. Газ хроматографиясының қолданысы жалынмен иондау детекторы (FID) дамығаннан кейін тез өсті.[6]
GC арқылы талдау[өңдеу | қайнарын өңдеу]
Газ хроматографы - күрделі үлгідегі химиялық заттарды бөлуге арналған химиялық талдау құралы. Газ хроматографы баған деп аталатын, газ ағыны өтетеін жіңішке түтікті пайдаланады. Үлгідегі қосылыстар әртүрлі химиялық және физикалық қасиеттеріне байланысты және стационарлы фаза деп аталатын материалмен әрекетесуіне байланысты баған бойымен әртүрлі жылдамдықта қозғалады. Химиялық заттар бағаннан шыққан кезде, олар электронды түрде анықталады және сәйкестендіріледі. Бағандағы стационарлы фазаның мақсаты қоспадағы компоненттерді бөлу. Оның арқасында компоненттердің әрқайсысы бағаннан әртүрлі уақытта (тежелу уақыты) шайылып шығады. Тежелу ретін немесе уақытын өзгерту үшін қолдануға болатын басқа параметрлер - тасымалдаушы газдың ағын жылдамдығы, бағанның ұзындығы мен температурасы.
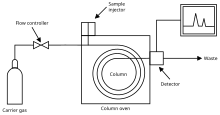
GC арқылы талдау кезінде, сұйық немесе газ түріндегі аналит әдетте микрошприцті (немесе, қатты фазалы микроэкстракция талшықтары, газ көзін ауыстыру жүйесін) пайдаланып, бағанның «басына» айдалады. Тасымалдаушы газ баған арқылы аналит молекулаларын жылжытады, бұл қозғалысты аналит молекулаларының адсорбциясы тежейді. Молекулалардың баған бойымен қозғалу жылдамдығы адсорбция күшіне байланысты, бұл өз кезегінде молекуланың түріне және стационарлы фазаның материалдарына байланысты болады. Әрбір молекуланың жылжу жылдамдығы әр түрлі болғандықтан, қоспаның компоненттері бөлініп, олар бағанның соңына әр түрлі уақытта жетеді (тежелу уақыты). Бағаннан шығыс ағынын бақылау үшін детектор қолданылады; осылайша, әрбір компоненттің шығатын уақыты мен оның мөлшерін анықтауға болады. Әдетте заттарды сапалық анықтау үшін бағаннан шығу реті не тежелу уақыты қолданылады.
Аспап бөлшектері[өңдеу | қайнарын өңдеу]
Аутосамплерлер[өңдеу | қайнарын өңдеу]
Аутосамплерлер үлгіні инлетке автоматты түрде енгізуге мүмкіндік береді. Үлгіні қолмен енгізу мүмкін болғанымен, қазіргі кезде көп таралмаған. Автоматты түрде енгізу қайталанғыштықты жақсартады және уақытты тимді пайдалануға көмектеседі.

Әр түрлі аутосамплерлер бар. Аутосамплерлерді робот технологияларына қарай (ең көп таралғандары: XYZ роботы[7] және айналмалы роботтар) сыйымдылығына қарай (ауто-инжекторлар және аутосамплерлер) немесе үлгі түріне қарай жіктеуге болады:
- Сұйық
- Статикалық бу фазасы
- Динамикалық бу фазасы
- Қатты фазалы микроэкстракция (SPME)
Инлеттер[өңдеу | қайнарын өңдеу]

Бағанның инлеті (немесе инжекторы) үлгіні тасымалдаушы газдың үздіксіз ағымына енгізуге мүмкіндік береді. Инлет - бағанның басына бекітілген аспаптық бөлік.
Инлеттің негізгі түрлері:
- S/SL (сплит/сплитсіз) инжектор; үлгі қыздырылған шағын камераға шприц арқылы септумды тесіп енгізіледі - жылу үлгіні және үлгі матрицасының булануын жеңілдетеді. Содан кейін тасымалдаушы газ үлгіні толығымен (сплитсіз режим) немесе үлгінің бір бөлігін ғана (сплит режимі) бағанға айдайды. Сплит режимінде, енгізу камерасындағы көмей арқылы үлгі/тасымалдаушы газ қоспасының бір бөлігі шығарылады. Талдаудың жоғары концентрациясы бар үлгілермен жұмыс жасау кезінде (>0,1%) сплитті енгізу қолданылады, ал сплитсіз енгізу аз мөлшердегі аналиттерді (<0,01%) талдауға ыңғайлы. Сплитсіз режимде жүйені ластайтын ауыр компоненттерден тазарту үшін алдын ала белгіленген уақыттан кейін енгізу камерасындағы көмей ашылады. Бұл алдын ала белгіленген уақытты бейімдеген жөн, қысқа уақыт (мысалы, 0,2 мин), шыңның дұрыс болуын қамтамасыз етеді, бірақ детектор жауабы жоғалады, ұзақ уақыт (2 мин) шыңның "құйрығын" ұзартады, бірақ сигналды да арттырады.[8]
- Бағандағы инлет; сынама бағанға толығымен қыздырусыз, еріткіштің қайнау температурасынан төмен температурада енгізіледі. Төмен температура үлгіні тар аймаққа жинайды. Содан кейін баған мен инлетті қыздырып, үлгіні газ фазасына жіберуге болады. Бұл хроматография үшін ең төменгі температураны қамтамасыз етеді және үлгілерді олардың қайнау температурасынан жоғары температураларда ыдырауға жол бермейді.
- PTV инжекторы; Температурасы бағдарламаланған үлгіні енгізуді алғаш рет 1979 жылы Фогт сипаттады. Бұл алғашында капиллярлы GC-ға үлгінің үлкен көлемдерін (250 мкл дейін) енгізу үшін дамытылған әдісі болды. Фогт үлгіні бекітілген енгізу жылдамдығымен лайнерге айдады. Лайнердің температурасы еріткіштің қайнау температурасынан сәл төмен болды. Сәл қайнап жатқан еріткіш үздіксіз буланып, сплит көмейі арқылы шығарылды. Осы әдістің негізінде Пой Бағадарламаланатын Температуралы Буландырғыш (PTV) инжекторын ойлап тапты
- Газ көзі инлеті не газ көзін ауыстыру жүйесі.
- P/T (бөліп тұзақтау) жүйесі; Инертті газ су ерітіндісі арқылы көпіршіп өтіп, ерімейтін ұшқыш химиялық заттарды матрицадан бөледі. Ұшқыш заттар адсорбентпен толтырылған бағанға (тұзақ, концентратор) қалыпты температурада «тұзақталады». Содан кейін бағанды қыздырады және ұшқыш заттарды газ ағынына тасымалдайды. Концентрлеуді немесе тазартуды қажет ететін үлгілерді, әдетте, S/SL портына жалғанған осындай жүйе арқылы енгізуге болады.
Тасымалдаушы газды (жылжымалы фазаны) таңдау өте маңызды. Сутектің тиімділігі жағынан гелиймен салыстыруға болатын ағындардың ауқымы үлкен. Алайда, ағым жылдамдығы бейімделген болса, гелий тиімдірек болады, және ең жақсы бөлінуді қамтамасыз етеді. Гелий жанбайды және көптеген детекторлармен және ескі құралдарда жұмыс істейді. Сондықтан, гелий - ең көп таралған тасымалдаушы газ. Алайда, гелийдің бағасы соңғы жылдары айтарлықтай өсті, бұл ғалымдардың көбін сутегі газына ауысуға мәжбүр етті.
Детекторлар[өңдеу | қайнарын өңдеу]
Ең жиі қолданылатын детекторлар - жалынмен иондау детекторы (FID) және жылу өткізгіштік детекторы (TCD). Екеуі де компоненттердің көбіне сезімтал және екеуі де концентрацияның кең ауқымында жұмыс істейді. TCD-лар іс жүзінде әмбебап болып табылады және оны тасымалдаушы газдан басқа кез келген компоненттерді анықтау үшін қолдануға болады (жылу өткізгіштігі тасымалдаушы газдан өзгеше болса), FID бірінші кезекте көмірсутектер үшін қолданылады және оларға TCD-ға қарағанда сезімтал. Алайда FID суды анықтай алмайды. Екі детектор да айтарлықтай сенімді. TCD ыдыратпайтын детектор болғандықтан, оны FID алдында қолданып, сол аналиттердің толық анықталуын қамтамасыз етуге болады.[9] Басқа детекторлар тек заттардың белгілі бір түрлеріне ғана сезімтал немесе концентрациялардың тар ауқымында ғана жақсы жұмыс істейді.
Жылу өткізгіштік детекторы (TCD) вольфрам-рений филаменті арқылы өтетін заттың жылу өткізгіштік қабілетіне сүйенеді.[10] Бұл қондырғыда гелий немесе азот жоғары жылу өткізгіштігі арқасында тасымалдаушы газ ретінде қызмет етеді, олар филаментті суытып, біркелкі кедергі мен филаменттің электрлік тиімділігін қамтамасыз етеді.[11] Алайда, аналит молекулалары бағаннан шыққанда, жылу өткізгіштік күрт төмендейді, бұл детектордың жауабын тудырады. Жауап жылу өткізгіштіктің төмендеуіне байланысты, себебі бұл температураның жоғарылауына әкеледі, ал бұл өз кезегінде филаменттің кедергісін арттырады.[10] Детектордың сезімталдығы филаменттегі тоқ күшіне пропорционал, ал ол детектордың қоршаған орта температурасына және тасымалдаушы газдың ағын жылдамдығына кері пропорционал.[10]
Жалынмен иондау детекторында (FID) бағаннан шыға беріс жеріне жақын орналасқан сутегі ауамен жанатын жалынға электродтар орналастырылады, ал көміртегі бар қосылыстар бағаннан шыққан кезде олар жалынмен пиролизденеді.[10][11] Бұл детектор органикалық заттар не көмірсутектері бар қоспалар үшін ғана жұмыс істейді, өйткені көміртек пиролиз кезінде электродтар арасында ток тудыратын катиондар мен электрондар түзе алады.[10][11] Тоқ үшінің артуы тіркеліп, хроматограмманың шыңы ретінде көрінеді. FID-лерде анықтау шегі төмен (секундына бірнеше пикограмм), бірақ олар карбонилді көміртектен иондар түзе алмайды.[10] FID үшін жарайтын тасымалдаушы газдарға гелий, сутегі, азот және аргон жатады.[10][11]
Сілтілік жалын детекторы (AFD) немесе сілтілік жалынмен иондау детекторы (AFID) NPD тәрізді азот пен фосфорға жоғары сезімталдыққа ие. Алайда сілтілік металл иондары жалынның үстіндегі түйірден емес, сутегі газымен шығады. Осы себепті AFD NPD сияқты «шаршамайды», және ұзақ уақыт бойына тұрақты сезімталдықты қамтамасыз етеді. Сонымен қатар, сілтілік иондар жалынға қосылмаған кезде, AFD стандартты FID сияқты жұмыс істейді. Каталитикалық жану детекторы (CCD) жанғыш көмірсутектер мен сутекті өлшейді. Разрядтаумен иондау детекторы (DID) иондау үшін жоғары вольтты электр разрядын пайдаланады.
Полиарк реактор - бұл FID арқылы анықтамас бұрын барлық органикалық қосылыстарды метан молекулаларына түрлендіретін GC-FID құралдарына қосымша. Бұл әдісті FID сигналын жақсарту үшін қолдануға болады және көбірек көміртекті қосылыстарды табуға мүмкіндік береді.[12] Қосылыстардың метанға толық конверсиясы калибрлеу мен стандарттардың қажеттілігін жояды, өйткені барлық қосылыстардың жауап факторлары бірдей. Бұл күрделі қоспаларды жылдам талдауға мүмкіндік береді.
Жалын фотометрлік детекторы (FPD) қосылыстардың жану барысындағы спектральды сызықтарын анықтау үшін фотокөбейткіш түтігін қолданады. Колоннадан шығарылатын қосылыстар белгілі бір элементтерді қоздыратын сутегі жалынына түседі, ал қозған элементтер (P, S, галогендер, кейбір металдар) белгілі бір толқын ұзындығын шығарады.[11] Шығарылған жарық фотокөбейткіш түтігі арқылы сүзіледі және анықталады.[10][11] Атап айтқанда, фосфор шығаруы шамамен 510-536 нм және күкірттің шығуы 394 нм деңгейінде.[10][11] Атом эмиссиясы детекторында (AED) бағаннан шығарылатын үлгіні микротолқындар энергиялайтын плазмалы камераға түседі. Плазма аналитті ыдыратады, және белгілі бір элементтер атом эмиссиясының спектрін тудырады. Атом эмиссия спектрлері дифракциялық тормен дифракцияланады және бірнеше фотокөбейткіш түтіктері немесе фото диодтар арқылы анықталады.[11]
Электронды ілу детекторы (ECD) электронды ілу дәрежесін өлшеу үшін радиоактивті бета бөлшектерін (электронды) пайдаланады.[10][11] ECD құрамында галогендер, карбонил, нитрилдер, нитро топтары және органометаллдар сияқты функционалды топтары бар және электртеріс элементтері бар молекулаларды анықтау үшін қолданылады.[10][11] Детектордың бұл түрінде жылжымалы фазадағы тасымалдаушы газ ретінде азот немесе аргондағы 5% метан қолданылады. Тасымалдаушы газ бағанның соңында орналасқан екі электродтың арасынан өтеді, ал катод жанында (теріс электрод) 63Ni сияқты радиоактивті фольга орналасады.[10][11] Радиоактивті фольга бета бөлшегін (электронды) шығарады, ол тасымалдаушы газбен соғысып, оны иондап, тоқ күшін тудырады. Электртеріс элементтері немесе функционалды топтары бар молекулалар электронды іліп алады да, тоқ күшін төмендетеді, бұл детектор жауабын тудырады.[10][11]
Азот-фосфор детекторы (NPD), термоэлектрондық детектордың бір түрі, онда азот пен фосфор арнайы жабылған шарда Шығу жұмысын өзгертеді және нәтижесіндегі ток өлшенеді.
Құрғақ электролиттік өткізгіштік детекторында (DELCD) ауа фазасы мен жоғары температура қолданылады. Хлорланған қосылыстарды өлшеуге арналған.
GC-MS деп аталатын бұл әдіс масс-спектрометрді (MS) қолданады; өте тиімді және сезімтал, тіпті аз мөлшердегі қосылыстарды анықтайды. Бұл детекторды хроматограммалардағы аналиттерді олардың массалық спектрі бойынша анықтау үшін пайдалануға болады.[13] Кейбір GC-MS резервтік детектор ретінде әрекет ететін ЯМР спектрометріне қосылған. Бұл комбинация GC-MS-ЯМР ретінде белгілі. GC-MS-ЯМР-ға қосылған инфрақызыл спектрофотометр қосымша детектор ретінде әрекет етеді. Бұл комбинация GC-MS-NMR-IR ретінде белгілі. Алайда, бұл өте сирек кездесетіндігін атап өту керек, өйткені көптеген талдауларды тек GC-MS арқылы жасауға болады. Вакуумдық ультракүлгін (VUV) газ хроматографиясының детекторларындағы ең соңғы дамыған түрі. Химиялық бөлшектердің көпшілігінде шамамен 120–240 нм аралығында бірегей абсорбция спектріне ие. Егер абсорбцияның спектрлері аналиттер үшін белгілі болса, VUV детекторы химиялық кедергілер болмаған кезде ағымдағы молекулалар санын абсолютті (калибрлеусіз) анықтауға қабілетті.[14]
Бұдан басқа детекторлар: Холл электролиттік өткізгіштік детекторы (ElCD), гелиймен иондау детекторы (HID), инфрақызыл детектор (IRD), фото-иондау детекторы (PID), импульсті разрядтпен иондау детекторы (PDD) және термионды иондау детекторы (TID).[15]
Әдіс дайындау[өңдеу | қайнарын өңдеу]

Әдіс дегеніміз белгілі бір талдауды жүргізуге арналған GC параметрлерінің жиынтығы. Әдіс дайындау деп берілген талдауды барынша жақсы орындауға арналған GC параметрлерін анықтау процессін айтамыз. Оңтайландыруды қажет ететін параметрлерге көбіне инлет температурасы, детектор температурасы, бағанның температуралық бағдарламасы, тасымалдаушы газ бен оның ағын жылдамдығы, бағанның станционарлы фазасы, диаметрі, ұзындығы, инлеттің типі, үлгінің енгізілетін мөлшері, енгізу әдісі жатады. Детектордың түріне байланысты, оның параметрлері де әртүрлі болады және оңтайландыруды қажет етеді. Кейбір GC-лерде тасымалдаушы ағынның бағытын өзгертуге арналған клапандар болады. Олардың ашылып-жабылатын уақытын оңтайландыру да әдіс дайындаудың маңызды бөлігі.
Тасымалдаушы газ бен оның ағын жылдамдығын таңдау[өңдеу | қайнарын өңдеу]
Ең жиі қолданылатын газдарға гелий, азот, аргон, сутек and ауа жатады. Қай тасымалдаушы газды қолдану керек екені детекторға байланысты. Мысалы, разрядтаумен иондау детекторы гелийды талап етеді. Кейде үлгінің матрицасы тасымалдаушы газды таңдау барысында үлкен рөл ойнайды. Мысалы, егер талданып жатқан үлгілер аргонда дайындалса, тасымалдаушы газ да аргон болғаны абзал. Қауіпсіздік ережелері мен қолжетімділік те таңдауға әсер етеді. Мысалы, сутек жанғыш газ, сондықтан оны қолдану қауіп тудыруы мүмкін, ал өте таза гелий кей жерлерде қолжетімді емес, әрі бағасы да қымбат. Оған қоса, гелийдің жетіспей бастады, сондықтан көптеген лабораториялар гелийді сутекпен алмастыруға көшті. Тасымалдаушы газдың тазалығы да детекторға сай таңдалады, дегенмен жоғары сезімталдық үшін барынша таза газдарды пайдаланған абзал. Көбінесе 99.995% не одан да таза газдар қолданылады. Заманауи аспаптардың көбісі 5-деңгейлі тазалықты талап етеді, бұл деген 99.999% таза газдар. Бұл олардың құрамындағы қоспалардың концентрациясы 10 ppm шамалас дегенді білдіреді. Қолданыстағы ең жоғары тазалық теңгейі 6 (99.9999%) болып саналады, дегенмен кейбір мақсаттарда 7-деңгейлі тазалықтағы газдар да қолданылады. Тасымалдаушы газдың сызықтық жылдамдығының әсері температура әсеріне ұқсас. Сызықтық жылдамдық неғұрлым жоғары болса, соғұрлым талдау тезірек жүреді, бірақ аналиттер арасындағы бөліну төмендейді. Сызықтық жылдамдықты таңдау - бұл бөліну өнімділігі мен талдау ұзақтығы арасындағы тепе-теңдікті табу. 1990-жылдарға дейін шыққан аспаптарда тасымалдаушы газдың ағын жылдамдығы инлеттегі қысым арқылы басқарылды. Нақты ағын жылдамдығы шығу көмейінде орналасқан флоу-метр арқылы анықталды. Бұл процесс ұзақ уақытты талап етті және өте күрделі әрі шаршататын процедура болды. Талдау барысында қысымды өзгерту мүмкін емес, сондықтан талдау барысында ағын жылдамдығын өзгерту мүмкін емес еді. Инлеттегі қысым мен ағын жылдамдығын сығылатын сұйықтықтарға арналған Хаген-Пуазейль теңдеуі арқылы сипаттауға болады. Дегенмен заманауи аспаптар ағын жылдамдығын аутоматты түрде өлшейді, және оны электронды түрде басқаруға болады. Оған қоса, ағын жылдамдығын талдау барысында өзгертіп, қысым бағдарламаларын жасауға болады.
Станционарлы фазаны таңдау[өңдеу | қайнарын өңдеу]
Еріген заттың полярлығы стационарлы фазаны таңдау барысында өте маңызды. Ең дұрысы баған полярлығы талданып жатқан заттың полярлығына ұқсас болғаны абзал. Ашық түтікті бағандардағы көп таралған станционарлы фазалар цианопропилфенил диметил полисилоксан, полиэтиленгликоль, бис-цианолпроил цианопропилфенил полисилоксан, дифенил диметил полисилоксан жатады. [10]
Инлет типі және ондағы ағын жылдамдығы[өңдеу | қайнарын өңдеу]
Инлет түрі көбіне үлгінің күйіне байланысты таңдалады. Сұйық үлгілер бағандағы инлет көмегімен тікелей бағанға енгізіле алады. Егер еріткіш матрицасы буландыруды талап етсе S/SL инжекторлары қолданылады. S/SL инжекторлары қазіргі кезде ең көп қолданылатын инлет типі. Газ үлгілер көбіне газ көзін ауыстыру инжекторларының көмегімен енгізіледі. Адсорбцияланған үлгілер (мысалы адсорбциялық түтіктер) көбіне бағанмен байланысқан не байланыспаған шеткі жүйелерде десорбцияланады (мысалы бөліп-тұзақтау жүйелері). Қатты фазамен микроэкстрациялау (ҚФМЭ, SPME) талшықтары тікелей S/SL инлетінде десорбциялана алады.
Енгізілетін үлгі мөлшері мен енгізу әдісі[өңдеу | қайнарын өңдеу]
Үлгіні енгізу[өңдеу | қайнарын өңдеу]
Хроматографиялық талдау үлгі бағанға енген сәтте басталады. Капиллярлы газ хроматографиясының дамуы үлгіні енгізуді қиындата түсті. Бағандағы инлет арқылы үлгіні енгізу әдісі толтырылған бағандармен жақсы жұмыс істесе де, бұл әдісті капиллярлы бағандармен қолдану мүмкін емес, себебі енгізілген үлгі мөлшері бағанды артық жүктемеуі қажет, ал енгізілген үлгінің бағандағы ені хроматография әсерінен жайылуға байланысты кішкентай болуы тиіс. Бұл шарт орындалмаған жағдайда, хроматографиялық бағанның өнімділігі (заттарды бөлу қабілеті) күрт төмендейді. Көп жағдайда енгізілетін үлгінің көлемі мен детектор ұясының көлемі аналит молекулалары бар элюат көлемінің 1/10 бөлігі болуы тиімді.
Үлгіні енгізудің жақсы әдісі бағанда тиімді бөліну өнімділігін, репрезентативті үлгілердің дәл әрі қайталанғыштығы жоғары енгізілуін, үлгінің құрамын аналиттердің қайнау температурасына, полярлығына, концентрациясы мен термал/катализдік тұрақтылығына қарамай, өзгертпей енгізілуін қамттамасыз ететін, сұйылтылмаған үлгілерге де, іздік концентрацияларға да сай келетін болуы тиіс.
Дегенмен, микролитрлік шприцтерді қолдану көптеген проблемаларға әкеліп соғады. Нарықтағы ең жақсы шприцтердің өзі тек ең кем дегенде 3%-дық дәлдік көрсетеді, ал қолы үйренбеген адамдар қолданған кезде, қателіктер арта түседі. Мысалы, шприцті енгізу кезінде ол септумның бір бөлігін іліп алып кетуі мүмін. Ол иненің ұшын бұғаттап, келесі енгізу барысында үлгінің көлемін азайтады, ал мұны бірден анықтау қиын. Оған қоса үлгідегі аналиттің бір мөлшері септум жасалған материалға тұзақталып қалуы мүмкін. Бұл жағдайда, келесі талдау кезінде жалған шыңдар пайда болады. Ұшқыш компоненттер енгізу барысында ине ұшынан буланып кетуі де ғажап емес, бұл компоненттердің үлгідегі мөлшерін азайтады. [16]
Баған таңдау[өңдеу | қайнарын өңдеу]
Бағанды көбіне үлгі мен өлшеніп жатқан объектке сай таңдайды. Бағанды таңдау барысында қарастыратын негізгі химиялық параметр - қоспаның полярлығы. Үлгінің полярлығы стационарлы фазаның полярлығына ұқсас болған сайын, бөліну өнімділігі арта түседі, дегенмен талдау уақыты да онымен бірге артады. Бөліну мен талдау уақыты одан басқа стационарлы фазаның көлеміне, бағанның диаметрі мен ұзындығына да байланысты.
Баған температурасы мен оның бағдарламасы[өңдеу | қайнарын өңдеу]

Газ хроматографындағы баған(дар) температурасы электронды түрде өте дәл қадағаланатын пеште орналасады. Көп жағдайда баған температурасы деп дәл осы пеш температурасын айтады. Шынында бұл екеуі әр түрлі термин болғанымен, көп жағдайда олар бірін-бірі алмастыра алады.
Аналиттің бағаннан ағып шығу жылдамдығы баған температурасына тура пропорционал. Температура жоғарлаған сайын, үлгі соғұрлым баған бойымен тез қозғалады. Дегенмен, анаилттердің қозғалу жылдамдығы артқан сайын, олардың бөлінуі азая түседі, себебі олар стационарлы фазамен әрекеттесіп үлгермейді.
Жалпы, температураны бөлінуге әсер етпей, бірақ талдау уақытын барынша азайтып таңдайды.
Баған температурасы талдау барысында тұрақты болып қалатын әдістерді изотермалық әдістер деп атайды. Шындығында, көптеген әдістер талдау барысында пешті қыздырады не суытады, белгілі бір уақытқа тұрақты қылып ұстайды және т.б. Талдау барысындағы температураның өзгеруін пештің температурасының бағдарламасы деп атайды.
Температура бағдарламасы бөліну өнімділігін сақтап, талдау уақытын азайтуға мүмкіндік береді.
Нәтижелерді өңдеу мен талдау[өңдеу | қайнарын өңдеу]
Сапалық талдау[өңдеу | қайнарын өңдеу]
Хроматография нәтижелері көбіне детектор жауабының уақыт бойынша функциясы (хроматограмма) түрінде беріледі. Ондағы әр шың қоспаның құрамындағы әр аналитке сәйкес келеді. Әдістің жағдайлары бір болған кезде, шыңдардың тежелу уақыты мен жалпы бейнесі тұрақты болып сақталады, сондықтан оны аналиттерді сәйкестіндіруге қолдануға болады. Дегенмен, жаңа әдістердің көбінде, GC масс-спектрометр тәрізді аналиттерді сапалық анықтауға болатын детекторға жалғанады. Бұл аналиттердің тез, артық жұмыссыз анықтауға мүмкіндік береді.
Сандық талдау[өңдеу | қайнарын өңдеу]
Хроматоргаммадағы шыңның ауданы аналит мөлшеріне пропорционал. Сондықтан да, шың ауданын интегралдау арқылы есептеп, ол арқылы аналиттің концентрациясын табады. Аналиттің әртүрлі белгілі концентрациясына детектордың жауабын тауып, оны мөлшерлеу қисығы арқылы белгісіз концентрацияны есептеуге қолдануға болады. Кейде, концентрацияны табу үшін аналиттің салыстырмалы жауап факторын да есептейді. Салыстырмалы жауап факторы дегеніміз детектордың мөлшері белгілі аналит және қосылған ішкі стандартқа (қоспаға белгілі мөлшерде қосылған, тежелу уақыты белгілі зат) берген жауаптарының қатынасы. Жаңа GC-MS жүйелерінде, хроматографияға арналған бағдарламалар шыңдарды интегралдау, масс-спектрлерді сәйкестендіру тәрізді жұмыстарды адам қатысынсыз, өзі атқарады.
Дереккөздер[өңдеу | қайнарын өңдеу]
- ↑ a b c Pavia, L., Gary M. Lampman, George S. Kritz, Randall G. Engel Introduction to Organic Laboratory Techniques (4th Ed.) — Thomson Brooks/Cole, 2006. — P. 797–817. — ISBN 978-0-495-28069-9.
- ↑ Gas Chromatography. Linde AG. Басты дереккөзінен мұрағатталған 3 наурыз 2012. Тексерілді, 11 наурыз 2012.
- ↑ Grob Carrier Gases for GC. Restek Advantage, Restek Corporation (1997). Тексерілді, 9 наурыз 2016.
- ↑ Berichte der Deutschen Botanischen Gesellschaft v.24 1906. (ағыл.).
- ↑ Ettre, Leslie S. (2008), The Beginnings of Gas Adsorption Chromatography 60 Years Ago, LCGC North America, http://www.chromatographyonline.com/beginnings-gas-adsorption-chromatography-60-years-ago?id=&sk=&date=&%0A%09%09%09&pageID=4
- ↑ R. A. Dewar; McWILLIAM, I. G. (March 1958). "Flame Ionization Detector for Gas Chromatography" (in en). Nature 181 (4611): 760. Bibcode 1958Natur.181..760M. doi:10.1038/181760a0. ISSN 1476-4687.
- ↑ Carvalho, Matheus (2018). "Osmar, the open-source microsyringe autosampler". HardwareX 3: 10–38. doi:10.1016/j.ohx.2018.01.001.
- ↑ Chasteen Split/Splitless and On-Column Gas Chromatographic Injectors. Тексерілді, 6 қазан 2019.
- ↑ Gas Chromatography. ACRF. Тексерілді, 11 наурыз 2012.
- ↑ a b c d e f g h i j k l m n Harris Daniel C. 24. Gas Chromatography // Quantitative chemical analysis — Fifth. — W. H. Freeman and Company, 1999. — P. 675–712. — ISBN 978-0-7167-2881-8.
- ↑ a b c d e f g h i j k l Higson S. Analytical Chemistry. — OXFORD University Press, 2004. — ISBN 978-0-19-850289-0.
- ↑ Quantitative carbon detector (QCD) for calibration-free, high-resolution characterization of complex mixtures.
- ↑ Fundamentals of analytical chemistry — Ninth. — Belmont, CA. — ISBN 9780495558286.
- ↑ Schug, Kevin A.; Sawicki, Ian; Carlton, Doug D.; Fan, Hui; McNair, Harold M.; Nimmo, John P.; Kroll, Peter; Smuts, Jonathan et al. (1834). "Vacuum Ultraviolet Detector for Gas Chromatography". Analytical Chemistry 86 (16): 8329–35. doi:10.1021/ac5018343. PMID 25079505.
- ↑ "Ionization-based detectors for gas chromatography". Journal of Chromatography A 1421: 137–153. 2015-11-20. doi:10.1016/j.chroma.2015.02.061.
- ↑ Modern Practice of Gas Chromatography (4th Ed.) — John Wiley & Sons, 2004. — ISBN 978-0-471-22983-4.