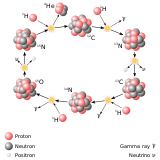
Ядроның нуклондық моделі
Протонның ашылуы
[өңдеу | қайнарын өңдеу]

Атом ядросы ашылғаннан кейін оның құрылымы қандай деген мәселе қойылды. 1919 ж. Э. Резерфорд α-бөлшектермен жасаған тәжірибелерін жалғастыра отырып, ядроның құрамына кіретін бірінші бөлшекті ашты.
Жабық ыдыс ішінде α-бөлшекті шығарушы элемент Ra радий және мырыш сульфидімен қапталған мөлдір Э экран бар (8.3-сурет). Жабық ыдыстан ауа сорылып шығарылған. α-бөлшектер экранға соқтығысып, жарқылдар туғызған. Ол жарқылдарды М микроскоп арқылы бақылаған. Келесі экспериментте ыдысты азот газымен толтырады. Енді а-бөлшектер өзінің энергиясын азоттың атомдарын иондауға және оларды қоздыруға жұмсап, экранға жете алмайды. Дегенмен, сирек болса да, экранда жарқылдар байқалған. Иондану кезінде пайда болатын электрондар ондай жарқылдарды туғыза алмайды. Ендеше α-бөлшек азот атомымен соқтығысқанда оның ядросынан белгісіз бір зарядталған бөлшекті ұшырып шығарған.
Магнит және электр өрістерінің осы белгісіз бөлшектерге әсерлерін зерттеу нәтижелері, оның оң электр заряды бар бөлшек екенін көрсетті және осы бөлшектің массасы сутегі атомы ядросының массасына тең болып шыққан. Осы тәжірибе басқа заттармен - фтор, натрий, бор, алюминий және т.с.с. қайталанды. Оларды α-бөлшектермен аткылағанда, әр кезде сутегі атомның ядросы ұшып шығады. Бұл, ядро құрамына сутегі атомы ядросының кіретінін дәлелдейді. Осы сутегі атомының ядросы протон деп аталды.
Протон оң зарядталған және заряды электронның элементар зарядына (е = 1,6 · 10−19Кл) тең. Протонның массасы
mр = 1,6726 · 10-27кг = 1,00728 м.а.б. = 938,27 МэВ.
Протонның ашылуы алғашқыда атом ядросының протон-электрондық моделін ұсынуға мүмкіндік берді. Бірақ тәжірибелер мен есептеулер атом ядросының протон мен электроннан құрылуы мүмкін емес екенін дәлелдеді.[1]
Нейтронның ашылуы
[өңдеу | қайнарын өңдеу]Ядроның құрамына кіретін тағы бір бөлшекті ашуға талпынғандар неміс ғалымдары В.Боте мен Г.Беккер. Олар 1930 жылы жасаған тәжірибелерінде литий мен берилийді а-бөлшектермен атқылағанда, протонның орнына өте нашар жұтылатын бөлшектер ұшып шығатынын байқайды. Бұл бөлшектер қалыңдығы 20 см болатын қорғасын қабатынан өтіп кеткен. Осы мәселемен француз ғалымдары Ирен және Фредерик Жолио-Кюрилер де айналысады. Олар бериллийді а-бөлшектермен атқылағанда пайда болатын сәуле жолына парафин пластинасын қойғанда, 8.4-суретте көрсетілгендей сутегіге қаныққан парафиннен протондар ұшып шығады деп болжам жасайды. Ағылшын ғалымы Дж. Чедвик осы жылы берилийді а-бөлшектермен атқылағанда одан бөлінетін табиғаты белгісіз сәуленің қасиеттерін зерттеу жұмыстарын жүргізеді.
Энергияның және импульстің сақталу заңдарына сүйене отырып, жүргізілген есептеулер нәтижесінде белгісіз бөлшектің массасын анықтайды. Чедвик бұл сәуленің электрлік бейтарап бөлшектер ағыны екенін дәлелдеген. Белгісіз бөлшектің массасы жуықтап алғанда протонның массасына тең болып шыққан. Атом ядросының құрамында протон сияқты ауыр, бірақ бейтарап бөлшектің бар болуы мүмкін деген батыл болжамды 1920 жылы Э. Резерфорд айтқан және оны нейтрон деп атауды ұсынған еді. Сонымен, жаңа бөлшек нейтрон деп аталды. Нейтронның электр заряды нөлге тең, сол себепті оның зат арқылы өтетін өтімділік қабілеті өте жоғары. Қазіргі дәл өлшеулер бойынша нейтронның массасы
mn = 1,6749 · 10-27 кг = 1,00866 м.а.б. = 939,56 МэВ.
Нейтрон символы арқылы белгіленеді, электр заряды жоқ, ал салыстырмалы атомдық массасы бірге жуық. Мына жағдайды айта кету керек, нейтронның массасы протонның массасынан 2,5 электрон массасына артық. Ұзақ уакыт бойы ауада да, жерде де нейтрон еркін күйінде кездеспеген. Тек 1950 жылы ғана осы құбылыстың сыры ашылды. Нейтрон — тұрақты бөлшек емес. Ядродан бөлініп шыққан нейтрон, 14 минуттай уақыт аралығында протонға, электрон және тыныштық массасы жоқ бөлшек — антинейтриноға өздігінен ыдырайды.[1]
Атом ядросының құрамы
[өңдеу | қайнарын өңдеу]1932 жылы нейтрон ашылғаннан соң, орыс ғалымы Д.Д. Иваненко мен неміс ғалымы В. Гейзенберг ядроның протон-нейтрондың моделі туралы болжам ұсынды. Қазіргі кезде атом ядросының протон-нейтрондық құрамы зерттеулер негізінде дәлелденген және ғылыми қабылданған даусыз ақиқат болып табылады. Қалыпты жағдайда атом электрлік бейтарап болатындықтан протонның заряды модулі бойынша электронның зарядына тең, яғни ядродағы протондардың саны атом қабықшасындағы электрондардың санына тең. Олай болса, протондар саны зарядтық санға (Z) тең болуы керек. Ядроның құрамына кіретін оң зарядты протон мен электрлік бейтарап нейтрондардың жалпы санын нуклондар деп атауға келісілген. Ядродағы нуклондардың жалпы саны А массалық сан деп аталады:
Осы өрнектен ядроның құрамына кіретін нейтрондар санын N анықтауға болады:
Ядроның құрамын сипаттау үшін, оның Менделеев кестесіндегі атомдық нөмірі Z пен массалық сан А қолданылады. Атомдағы электрондардың массасы ядро массасына қарағанда ескермеуге болатындай анағұрлым аз. Сондықтан атом ядросының массалық саны А бүтін санға дейін жуық дәлдікпен алынған химиялық элементтің салыстырмалы атомдық массасына тең. Атомдық реттік нөмірі Z, ал массалық саны А болатын химиялық элементтің ядросын деп белгілейді.
Протонды , ал нейтронды түрінде белгілейді. Протон сутегі атомының ядросы болғандықтан, оны кейде деп те белгілеуге болады. Атом ядросы деген терминнің орнына оның баламасы ретінде нуклидтер деген термин де кеңінен қолданылады.[1]
Изотоптар
[өңдеу | қайнарын өңдеу]Атом ядроларының массаларын дәл өлшеу химиялық элементтердің басым көпшілігінде зарядтық сандары бірдей, бірақ массалары әр түрлі атомдардың бар екенін көрсетті.
Ядролық зарядтары (реттік нөмірлері Z) бірдей, ал массалық сандары А әр түрлі элементтер атомдарын изотоптар (грекше isos— бірдей және topos — орын) деп атайды.
Мысалы табиғатта реттік нөмірі Z = 18 аргонның ядросы құрамында N = 18; 20; 22 нейтрондары бар үш изотопы кездеседі. Атом қабықшасындағы электрондарының сандары бірдей болғандықтан, изотоптардың химиялық қасиеттері де бірдей. Ал ядроның массалары әр түрлі, сондықтан изотоптардың физикалық қасиеттерінде айырмашылық бар.
Табиғаттағы ең ауыр элементтің бірі уран , , түрінде кездеседі. Ең жеңіл элемент сутегінде үш изотоп — , , және бар. Сутегінің жеңіл изотопы — протий, ал изотопы — дейтерий деп аталады. Дейтерийдің табиғи сутегінің құрамындағы үлесі 0,015%. Ол оттегімен қосылғанда ауыр су түзіледі. Сутегінің үшінші изотопын тритий деп атайды және ол табиғатта кездеспейді.
Массалық сандары А бірдей, зарядтық сандары Z әр түрлі нуклидтерді изобаралар (бірдей ауыр деген сөз) деп атайды.
Қазіргі кезде химиялық элементтердің бәрінің де изотоптары бар екені белгілі.[1]
Дереккөздер
[өңдеу | қайнарын өңдеу]- ↑ a b c d Физика: Жалпы білім беретін мектептің жаратылыстану-математика бағытындағы 11 сыныбына арналған оқулық /С. Түяқбаев, Ш. Насохова, Б. Кронгарт, т.б. — Алматы: "Мектеп" баспасы. — 384 бет. ISBN 9965-36-055-3
| Бұл мақаланы Уикипедия сапа талаптарына лайықты болуы үшін уикилендіру қажет. |